

2018年、京都大学はiPS細胞を使ったパーキンソン病治療の臨床試験を開始した。パーキンソン病に罹患すると脳内の神経細胞が失われ、運動機能に障害が出る。これまで、一時的な症状の緩和や進行を遅らせる対症療法しか存在しなかったが、iPS細胞やES細胞を使った細胞移植治療によって、ようやく根本的な治療の可能性が拓けてきた。本臨床試験の主任研究者であり脳外科医でもある京都大学iPS細胞研究所の髙橋淳教授に、脳疾患治療研究の最前線を伺った。
私たちの脳は、無数の神経細胞で構成されている。神経細胞は突起を伸ばしてネットワークを形作り、互いに情報を伝達しあうことで、生命活動を維持している。その働きが私たちにとって重要なのは言うまでもないだろう。病気や事故で神経細胞が大量に失われると、精神や体の機能は容易に損なわれてしまう。
パーキンソン病は、中脳と呼ばれる部分の「ドパミン神経細胞」が失われることで発症する難病だ。脳内のドパミンが足りなくなり、主に運動機能に障害が現れる。症状は50歳以降に現れることが多く、手足の震えや筋肉のこわばりなどが起こり、日常生活に支障が出る。パーキンソン病患者のドパミン神経細胞は加齢とともに失われ、症状は進行し続ける。神経細胞が失われる原因は現在でも分かっていない。

「私たちがこだわっているのは、神経回路を再構築できる神経細胞の作製です」と話す髙橋教授。iPS細胞研究所内にて。
パーキンソン病の治療の基本となるのは、薬物投与や脳内に電極を埋め込む手術法だ。しかし、どちらも残っている神経細胞の働きを高めるアプローチでしかなく、一時的に症状を緩和させることはできても、細胞が失われるにつれて効果が薄れていく。
髙橋教授は、パーキンソン病の根本的な治療法の開発を目指して研究を続け、現在臨床試験が行われている「細胞移植療法」にたどり着いた。この細胞移植療法について、髙橋教授は次のように説明する。
「細胞移植には、大きく分けて2つのアプローチがあります。ひとつ目は移植した細胞を薬のように使う方法です。必要な物質を分泌する細胞を作って脳に移植することで、必要な場所に必要な物質を届け、生体の再生を促すことができます。ただし、この方法では移植した細胞はいずれ消え、根本的な治療にはなりません。もうひとつのアプローチは、移植した細胞を脳の中に生着させ、そのまま神経として機能させる方法です。私たちが研究しているのは、後者の方です」
一時的に救援物資を補給するのではなく、脳の情報伝達を担う神経細胞を届けて生着させる。髙橋教授らの細胞移植療法が成功すれば、細胞が失われ続けるパーキンソン病患者の脳に、新たな細胞を補充する画期的な治療法となる。
この臨床試験は、地道な基礎研究の積み重ねによって実現した。まず、脳の中で神経回路を形成して機能する細胞を作るために、iPS細胞から、中脳に存在するドパミン神経細胞にできるだけ近づけた細胞を作り上げる必要があった。
また、最終的に人間の脳に移植するため、作り上げる細胞は、人体にとって安全なものでなければならない。万全を期するため、培養方法やiPS細胞の作製方法の改良、分化した細胞の確実な選別方法も開発した。移植先の脳の環境を整え、移植細胞が生着しやすくなるための薬物の研究も行った。サルを用いた実験も行い、他人の細胞を移植する場合に起こる免疫反応を抑える条件も詳細に調べた。
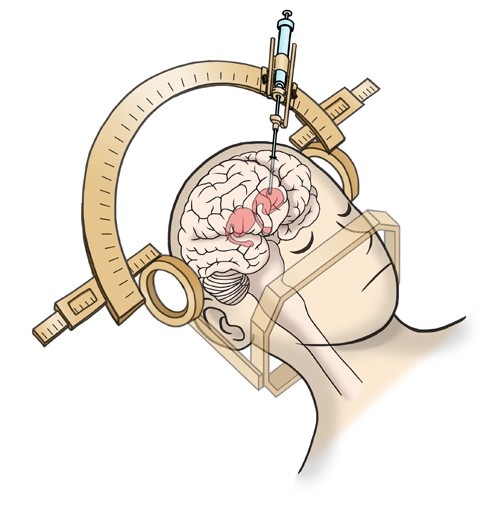
図1 ドパミン神経細胞を移植する手術の様子(図提供:iPS細胞研究所)
手術は頭部を固定したうえで頭蓋骨に直径12mmの穴を開け、そこから注射針のような器具を用い、細胞を注入する。
このようにして、課題をひとつひとつクリアし、安全性を確かめて、2018年についに患者の脳に移植する臨床試験までたどりついた。
移植の際には髙橋教授も手術室に入り、移植手術に立ちあった。だが、髙橋教授が起きている患者と顔を合わせることはないという。患者にプレッシャーを与えて心理的なバイアスが生じることを避けるためだ。
「研究は、もう私たちの手から離れました。ただ、臨床応用としては、これからが本当の勝負です。治療に有効かどうか。私たちの研究に審判を下すのは論文の審査員ではなく、患者さんです。もっと言えば、病気そのものなのです」
臨床試験は順調に進み、2020年末までに4例の手術を終えている。2021年中には、登録している患者7名すべての手術が終わる予定だ。移植後は免疫抑制剤を1年間服用してもらう。京大病院でフォローアップを行い、2年間の経過観察ののち、安全性と有効性を評価する。朗報を耳にする日を世界中の人々が心待ちにしている。
現在、髙橋教授は「大脳オルガノイド」を作製する研究も進めている。オルガノイドは実験室で作るミニ臓器だ。その大きさは数百ミクロンから数ミリ程度、髙橋教授らが作製した大脳オルガノイドも、2-3 mmのサイズだ。
「脳というよりは“神経細胞の塊”といったほうが正確です。ただし、ただの塊ではなく神経回路をもった塊です。オルガノイドは、生物が体を作りあげていくプロセスを人工的に再現して、iPS細胞やES細胞から三次元の構造を作ります。その作製過程で細胞同士の相互作用が起こり、自己組織化していきます。大脳オルガノイドは本物の大脳と同じように、層構造を作るので、神経細胞同士の複雑なネットワークも一緒に形成されるのです」
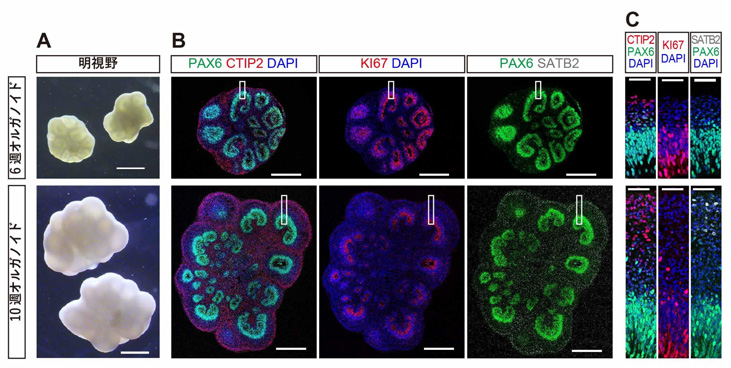
図2:ヒトES細胞から分化誘導した大脳オルガノイド。Aは分化誘導開始6週間後(上)と10週間後(下)を実体顕微鏡で見た写真。Bは細胞の種類によって違う色に染めた免疫染色像。CはBの縦長の白い四角部分を拡大した像。層構造ができているのがわかる。
スケールバー(横棒)は、A:1mm、B:500μm、C:50μm
出典:Kitahara T, Sakaguchi H, Morizane A, Kikuchi T, Miyamoto S, Takahashi J. Axonal extensions along corticospinal tracts from transplanted human cerebral organoids. Stem Cell Rep. 15(2): 467-481 doi: 10.1016/j.stemcr.2020.06.016 (2020)
髙橋教授が大脳オルガノイドを作るのは、単なる知的好奇心からではない。あくまで脳疾患の治療法開発のためだ。細胞移植を効果的に行うには、脳の中で正しく働く神経細胞を作る必要がある。それには、iPS細胞やES細胞から2次元で分化させるよりも、神経細胞が自己組織化されたオルガノイドを利用した方が成功しやすいと髙橋教授は考えている。
「大脳オルガノイドを作製してみると、複雑な神経活動が起きていることが分かりました。まず、大脳オルガノイドで機能的な神経ネットワークが形成されている可能性を実験的に確かめ、そのうえで、ヒトES細胞から作成した大脳オルガノイドをマウスの大脳皮質に移植する実験も行いました。すると、移植されたオルガノイドの神経細胞は突起を伸ばし、脊髄へ向かう経路に沿って伸展していきました」
これは、脳血管障害や頭部外傷で運動機能が障害された患者の治療法に結び付く画期的な成果だった。

コロナ禍で研究所内の人の出入りを制限していたため、オンラインで取材を実施した。
この結果を、髙橋教授は次のように振り返る。
「移植した細胞がここまで突起を伸ばすとは思ってもいなかったので、驚きました。もちろん、マウスでできたからといって、人間でできるとは限りません。それでも、誰かがチャレンジしないと研究は進みません。私はもともと外科医なので、脳梗塞や脳卒中の患者さんもたくさん見てきています。またパーキンソン病で、基礎研究から臨床応用までもっていった経験もあります。だから、私たちがやらないで誰がやるのかという思いで挑戦しています」
髙橋教授が脳に興味をもったのは、高校生のときだ。生きているヒトの脳を直接扱うためには脳外科医になるしかないと考え、医学部に進んだ。だが、当時の脳神経外科医が主に扱っていたのは脳血管障害や脳腫瘍だった。手術では、脳を傷つけないように血管を縫い合わせ、腫瘍を取り除く。皮肉なことに、いかに脳に触れないかが、脳外科の主要な命題だった。
「脳を直接扱いたくて脳神経外科に入ったのにちょっと違うなと思いました。が、てんかんの焦点を見つけて除去することによっててんかん発作を抑えたり、脳内に電極を挿入して刺激することによって体の動きをよくしたりする機能神経外科という分野があり、僕の興味に合いました。パーキンソン病に対する細胞移植治療を目指すのであればパーキンソン病に対する脳深部刺激手術も知らなければならないと思い、京大病院でまずこの手術を立ち上げました」
大学院に入ってからは、基礎研究と臨床の両方に取り組んだ。選んだ研究テーマは「再生医療」だ。髙橋教授が大学院に入ったのは1989年。iPS細胞どころかヒトES細胞も発見されていなかった時代に、先進的なテーマを選んだのは、指導教官である菊池晴彦教授が「これからは再生医療が大事だ」と主張したからだ。
「当時は欧米で中絶された胎児の細胞を移植する研究が行われていましたが、移植によって治療するには複数の中絶胎児が必要となり、手に入れることが難しいという問題がありました。そのころ、アメリカのソーク研究所で線維芽細胞の遺伝子を細工して移植する研究が行われていたので、その方法を学ぼうと思い、留学しました。ところが留学した先で、大人のネズミ脳の中に、神経幹細胞という未分化な細胞があることが発見されたのです」
神経幹細胞は培養でどんどん増やすことができ、かつ必要な神経細胞に分化させることができる。髙橋教授は、神経幹細胞の研究をすることを決めて帰国した。その1年後の1998年に、アメリカでヒトのES細胞がつくられ、日本でも京都大学再生医科学研究所の中辻憲夫教授らがヒトES細胞の樹立に成功した。これにより、ヒトの神経細胞を作製することが可能になった。それを受け、髙橋教授はES細胞を使って脳機能を再生する研究を進めた。
そして2007年には、山中伸弥教授がヒトiPS細胞を樹立した。iPS細胞は患者自身の細胞を使った免疫拒絶反応のない移植細胞を作製できる。これにより、脳疾患の治療においても、臨床応用の可能性がさらに大きく拓けることになった。
不思議なことに、髙橋教授の近くでは必要な技術革新がいくつもタイミングよく起こっている。おかげで髙橋教授は最先端の技術をいち早く導入し、臨床応用に繋げることができた。その軌跡を振り返ると、まるで誰かが髙橋教授に脳疾患治療の開拓を託し、行くべき道を案内しているかのようだ。

iPS細胞研究所の前で。研究所ができる前は野原だった。髙橋教授が大学院生のときは、よくここでキャッチボールをしていたそうだ。
現在、髙橋教授はiPS細胞研究所で多くの基礎研究のプロジェクトを走らせ、次々と論文を発表している。だが、脳神経外科医のマインドはひとときも忘れたことはないという。論文を書くためだけの実験を行ったことは一度もなく、常に治療を見据えて研究している。
取材の最後にiPS細胞研究所の設立の経緯について尋ねると、髙橋教授は懐かしそうに微笑んだ。
「iPS細胞に関する研究と臨床応用を行う研究所を作ろうという話で、京都にみんなで集まったのは2007年のクリスマスでした。僕を含む当時のメンバーが設計図を描いて、2010年に第一期棟が完成しました」
今のiPS細胞研究所は「総合商社」のようだと髙橋教授は話す。基礎研究から臨床応用まで、さまざまな分野の一流のプレイヤーがそろっているからだ。施設と仲間に支えられ、髙橋教授はこれからもとどまることなく、iPS細胞と脳疾患治療の可能性を拓き続けるのだろう。


iPS細胞に関する基礎研究および医療応用を目指して2010年4月1日に設立。分子細胞レベルでの新たな生命科学の分野を開拓する「未来生命科学開拓部門」、患者から提供された細胞をもとに作成したiPS細胞から病気のメカニズムを探り治療法を開発する「増殖分化機構研究部門」、iPS細胞からさまざまな細胞を分化させるための誘導方法を確立し、細胞移植治療法についての効果や安全性を評価する「臨床応用研究部門」、臨床応用に必要な法規制整備やiPS細胞の品質保証など共通基盤技術の開発を推し進める「基盤技術研究部門」、iPS細胞の臨床応用を取り巻く倫理的、法的、社会的な課題を整理し、対処法を検討する「上廣倫理研究部門」の5つの研究部門が設置されている。
【取材・文:寒竹泉美 撮影:吉田亮人】
 bana1.png (300px×80px)
bana1.png (300px×80px) bana1_e.png (300px×80px)
bana1_e.png (300px×80px) NovelPrize2015.png
NovelPrize2015.png