

感染症と人類との戦いの歴史は長い。多くの犠牲者を出しながら、人類は感染症をひとつずつ乗り越えてきた。その勝利の裏には、地道な研究を続けてきた科学者たちの努力がある。大阪大学微生物病研究所の堀口安彦教授もその一人。堀口教授は、感染症を引き起こす病原性細菌の研究に取り組んでいる。
細菌感染症は、抗菌薬の発明で治療が可能になり、ワクチンの開発により予防も可能になったことから、まるで解決してしまったかのように思われているが、堀口教授いわく、「細菌がどのように病態を引き起こすのかは、ほとんど解明されていない」とのこと。細菌感染症の最前線を、堀口教授に聞いた。
「毒」と聞くと、どんな物質を思い浮かべるだろうか。犯罪に使われたことのある「青酸カリ」や「サリン」、「ヒ素」の名を挙げる人が多いかもしれない。しかし、地球上でもっとも強力な毒は、小さな細菌が作り出す毒素である。
堀口教授は、細菌毒素の毒性の強さを学部生にわかりやすく伝えるために、毒物の1グラム当たりの推定致死人数を比較するグラフを作成した(図1参照)。このグラフによると、青酸カリが1グラムで殺せる人間の数は0.5人、サリンの前駆体であるDFPは100人、ヒ素は143人だ。一方、細菌が産出する毒素である破傷風菌毒素は100万人、ボツリヌス菌毒素は500万人。同じスケールのグラフでは表しきれないほど、強力であることが分かる。
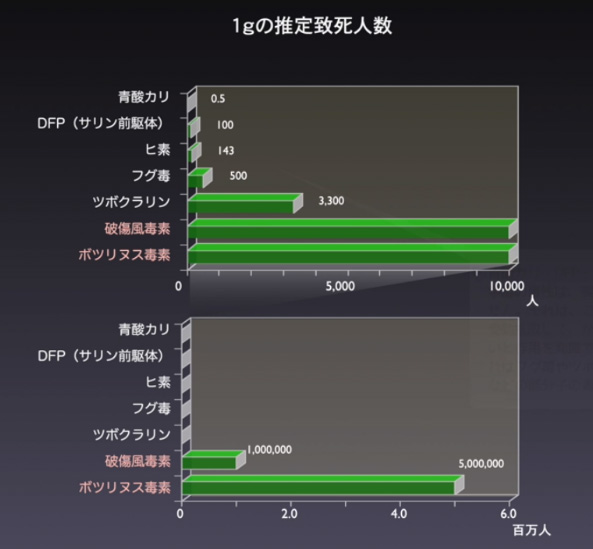
図1 毒物の1グラム当たりの推定致死人数(堀口教授作成)。横軸の最大値が1万人(上)と600万人(下)のグラフ。細菌毒素(赤字)と化学毒やその他の自然毒(白字)では毒力に圧倒的な差がある。ツボクラリンは南米の先住民が狩猟などで毒矢に使われてきた植物毒。
青酸カリのような化学毒は、体内の血液などに入って受動的に拡散し、一定の量を超えて初めて毒性を発揮する。しかし、細菌毒素は毒性を表すメカニズムが全く違うと堀口教授は説明する。
「細菌毒素は、自ら宿主の体内を移動して、標的となる細胞や分子に到達し、生体にとって重要な機能を担う分子を的確に狙い撃ちします。移動、侵入、攻撃という複数の機能を備えた多機能分子で、毒素単独で攻撃が完結するのです」
ウイルスや寄生虫は感染した場所で影響を及ぼすが、細菌の場合は、毒素を介して感染箇所から遠く離れた場所で病気を引き起こす例が数多くある。2000年に起きた雪印乳業のブドウ球菌食中毒事件は、時間も空間も超えて被害を引き起こす細菌毒素の特徴がよく分かる事例だ。集団食中毒が発生したのは関西地域だったが、原因は北海道工場の停電で黄色ブドウ球菌が発生したことだった。黄色ブドウ球菌の出す毒素が北海道で作られた脱脂粉乳に入りこみ、それを原料として生産した大阪工場の低脂肪乳が食中毒の原因となった。
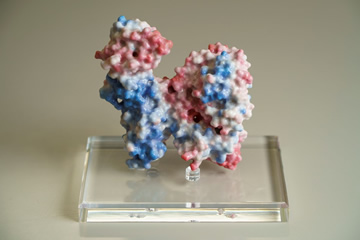
堀口教授のグループが立体構造を解明したパスツレラ菌毒素の3D模型。
このような重大な被害を引き起こす細菌毒素だが、その研究はあまり進んでいない。なぜなら、病原性細菌を発見して毒素を単離すれば、毒素を中和する抗体の製造が可能になり、治療ができるようになるからだ。治療さえできれば、毒素が病気を引き起こすメカニズムの解明は、差し迫った医療的課題ではなくなる。さらに、抗生剤で菌自体を殺すこともできるようになったため、細菌研究に対する社会の関心は薄れてしまった。
「私の10年以上先輩にあたる先生方に聞いた話ですが、抗生剤の登場が注目されていたころは、もうこれで解決だというムードがあったようです。他の分野の研究者から、緑膿菌や大腸菌のような固有の名前はもういらないだろう、抗生物質のアンピシリンが効く菌ならアンピシリンA、ゲンタマイシンが効くならゲンタマイシンBでいいじゃないかなんて言われるくらい、細菌の個性が無視されていたのです」
しかし、そのうち抗生剤が効かない薬剤耐性菌が現れ始めた。また、毒素を中和するだけでは発症や感染の流行を防ぐことができないケースも判明してくる。本当に細菌感染症から人々を救うためには、毒素を知り、病態を引き起こすメカニズムを解明することが重要だ。堀口教授は、それを長年にわたって主張し続けてきた。
堀口教授は、細菌毒素の構造と機能を解析し、病態を引き起こすメカニズムを解くことを目指してきた。その成果のひとつが、百日咳(ひゃくにちぜき)菌の出す「壊死毒素」の働きの解明だ。百日咳は名前が示すように、発作性の咳が出る感染症だが、稀に脳症を併発し、後遺症や死亡につながることが知られている。脳症の発症メカニズムはこれまで全く不明だったが、堀口教授たちの研究グループは、壊死毒素が神経に働き、脳症の発症に関与していることを示した。20年近く追い続けてきて、ようやく証明できた成果だった。
「時間がかかった一番の理由は、壊死毒素の毒性の発揮の仕方が特殊だったことにあります。細胞死を引き起こす毒素なら、ターゲットとなる細胞が死ぬことで毒素がどこに効いているのかを知ることができます。しかし、壊死毒素は細胞死を引き起こすのではなく、逆に細胞の働きを活性化するため、ターゲットとなる細胞を検出するのが技術的に難しかったのです」

さまざまな試行錯誤を行った堀口教授が、最終的にこの問題を突破できたのは、遺伝子工学に新しい技術が誕生したおかげだった。2006年に発表されたiPS細胞技術によって、実験に使用する毒素の作用解析のための細胞を比較的自由に作製できるようになった。また、2013年に報告されたCRISPR-Cas9技術によって、ターゲットとなる動物細胞の遺伝子改変を、より簡単に行えるようになった。どちらもノーベル賞を受賞した研究成果だが、これらによって堀口教授の研究は大きく前進したのである。
「技術革新の力は大きいですね。旧来からある遺伝子操作技術で壊死毒素の構造を一部改変し、CRISPER-Cas9のシステムを用いてターゲットとなる細胞の方も網羅的に遺伝子を改変しました。それにより、壊死毒素が結合する受容体分子を検出することができました。具体的には、細胞への侵入や受容体分子に結合する働きを持つ部分はそのままにして、結合したら細胞死が起こるような壊死毒素の変異タンパク質を作りました。これを作るだけで3年くらいかかりましたが、これとCRISPER-Cas9システムを組み合わせることで、壊死毒素のターゲットが神経細胞だということが判明したのです」

壊死毒素を脳内に投与したマウスは尾や後ろ足に麻痺が起こる。(図の提供:堀口教授))
神経細胞に効くのなら、脳で作用するのではないかと考えた堀口教授らは、壊死毒素をマウスの脳内に投与した。すると、マウスは脳症に特徴的な後ろ足の麻痺を発症した。脳症を起こしたマウスの脳を詳しく調べると、百日咳脳症の臨床所見とよく似ていることが分かった。この現象は百日咳菌が産生する他の毒素では見られず、百日咳脳症を引き起こしているのが壊死毒素であることを示す結果だった。
「これまで全く不明だった百日咳脳症の発症機構が示されたことで、脳症の予防や治療の可能性が大きく広がりました。百日咳菌ワクチンを含む三種混合ワクチンは、日本では生後3か月から接種しますが、接種前の乳児の感染が特に問題になっています。また、感染した場合は抗菌薬で治療を行いますが、脳症以外では咳発作についても発症メカニズムが分かっていないため、対症療法しかできません。細菌毒素の作用を明らかにすることで、症状を緩和や新たな治療法の開発が行えるようになると考えています」
堀口教授はいつから研究者を目指したのだろうか。そう尋ねると、意外な話が飛び出てきた。
「僕が大学受験する直前くらいに、カルビーからポテトチップスが売り出されてヒットしました。それがあまりにおいしかったものだから、これからジャガイモの需要が広まるぞと思ったのです。最初に大学の農学部に入ろうと考えたのは、ジャガイモの研究をやろうと思ったからでした。しかしよくよく調べてみたら、ポテトチップスのジャガイモは契約した農場で作られているため、自分が開発に関われる余地はあまりないと知りました」

堀口教授はよく若い研究者に対して、自分の師匠や先輩が研究していた菌はやるなと話す。誰も手をつけていない菌を研究するのは大変だが、研究者として「食べていく」ための戦略だ。
目標がなくなった堀口教授は、農学部のなかでは異質と思えた獣医学科に、特に獣医になる気はなかったのに進学した。さらに学部3年で研究室の配属を決めるときになると、冷暖房が完備されているからという理由で公衆衛生学教室を選んだ。そこが、たまたま細菌毒素を扱う研究室だった。
「ボツリヌス菌毒素は、自然界に存在する最も強力な毒だといわれていますが、動物実験でその効果を目の当たりにして衝撃を受けました。世の中になぜこのようなものが存在するのかと不思議に思い、そこから真面目に研究をするようになりました。熱心に実験をするようになったのは興味が湧いたからですが、扱いを一歩間違うと死んでしまいますから、真剣にやらざるを得ないわけです。ピペットもいまのように安全な道具は揃っていなかったので、ガラス管を口で吸い上げていました。指導も体育会系のノリで、そういう緊張感が好きでした」
「何も考えずに研究ばかりしてきた」と、堀口教授は40年近い研究生活を振り返る。
「定年後はもう研究から離れて趣味のロードバイクであちこち走りたいですね。でも、来年度も学生さんは来るし、しっかりと研究のスタンスを伝えて覚えてもらわないといけないなと思っています。細菌の生存に関係のない毒素がなぜ存在するのかという不思議も、まだ解き明かされていませんが、これはぜひ、これからの人にお願いしたいですね」


1934年に設置された、大阪大学で最初の附置研究所。微生物病をキーワードに、感染症、免疫、がんを中心に研究を展開する。80年以上もの歴史のなかで、病原体の発見やワクチンの開発など、数々の研究成果で生命科学の発展に貢献している。微生物が感染するメカニズムを探る「感染機構研究部門」、感染症から体を守るメカニズムを探る「生体防御研究部門」、がんの制御メカニズムを探る「環境応答研究部門」の3つを基幹部門とし、遺伝情報実験センターや難治感染症対策研究センターなど4つの付属施設をもつ。
【取材・文:寒竹泉美 撮影:大島拓也】
 bana1.png (300px×80px)
bana1.png (300px×80px) bana1_e.png (300px×80px)
bana1_e.png (300px×80px) NovelPrize2015.png
NovelPrize2015.png